Европейское агентство по лекарственным препаратам (European Medicines Agency, ЕМА) одобрило препарат Санкузо/ трансдермальная терапевтическая система гранисетрона (Sancuso/ Granisetron Transdermal System) компаний ПроСтракан Груп (ProStrakan Group plc) и 3M Драг Деливери Системс (3M Drug Delivery Systems).
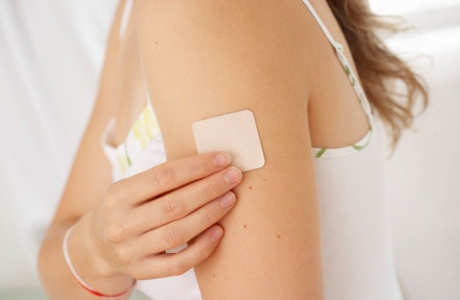
Компании ПроСтракан и 3M Драг Деливери Системс выпускают пластырь Санкузо в Европе
Как сообщает портал МЕДФАРМКОННЕКТ, компания ПроСтракан начала маркетинг лекарственного препарата Санкузо в этом месяце в Великобританию, Германию и Нидерланды.
ЧИТАЙТЕ ТАКЖЕ: FDA одобрило инъекционный антиэметик Ондансетрон компании BD Rx
Ожидается, что маркетинг препарата в другие европейские страны начнется в 2014 году. Впервые представленный в США в 2008 году, Санкузо является первым и единственным препаратом для лечения тошноты и рвоты, вызванными химиотерапией, который не нуждается в дополнительных таблетках или внутривенном введении.
ЧИТАЙТЕ ТАКЖЕ: В Европе одобрили препарат Лонквекс компании Тева для снижения длительности нейтропении при интенсивной химиотерапии
Данный препарат в виде трансдермального пластыря прикладывается к верхней части руки и носится около семи дней, обеспечивая продолжительное действие и избавляя пациентов от приема таблеток каждый день для контроля тошноты и рвоты, вызванных химиотерапией. Пластырь Санкузо доказал свою эффективность у пациентов, которые страдают от тошноты и рвоты при прохождении курсов химиотерапии.





 Як вибрати органічне овочеве пюре HiPP для вашої дитини?
Як вибрати органічне овочеве пюре HiPP для вашої дитини?  Бандаж на локоть: что это, и как выбрать
Бандаж на локоть: что это, и как выбрать  Пигментация кожи: что это? Как бороться с пигментацией
Пигментация кожи: что это? Как бороться с пигментацией  Как правильно выбрать массажер для ног?
Как правильно выбрать массажер для ног?  Топ лучших клиник Германии
Топ лучших клиник Германии
Только зарегистрированные пользователи могут оставлять комментарии
Войти